- Всю жизнь на таблетках?
- Больные не хотят пить лекарства
- Кокрановский обзор и другие опросы
- Почему пациенты боятся лекарств?
- В заключение
- Путь лекарства
- Путь лекарства
- Конкурс «био/мол/текст»-2018
- Да здравствует идея!
- Операция «Мишень»
- На поиски лигандов
- Сокращай, оптимизируй!
- Тестировали, тестировали, да вытестировали
- Выходи на рынок!
Всю жизнь на таблетках?
Поделиться:
— Доктор, сколько мне принимать эти таблетки?
— Всю жизнь!
— Всю? Так долго.
«Все лгут!» — заявлял незабвенный доктор Хаус. И врачи с этим, в целом, согласны. Но любой доктор хочет верить своему пациенту. Как часто больные заявляют, что они что угодно сделают, лишь бы восстановить свое здоровье… Все лгут?
Больные не хотят пить лекарства
На практике выясняется: «что угодно» — это выполнение лишь малой толики рекомендаций докторов.
Например, согласно исследованию, проведенному учеными из Калифорнийского университета в Сан-Франциско и Университета Северной Каролины в Чапел-Хилл, опубликованному в журнале «Circulation: Cardiovascular Quality and Outcomes», практически каждый третий больной скорее предпочтет раньше умереть, чем станет ежедневно принимать лекарства. В опросе приняли участие тысяча американцев среднего возраста (около 50 лет) со средним достатком, в гендерном отношении половину из них составили женщины, а в расовом — 63 % европеоиды.
Ученых интересовало, на что испытуемые готовы пойти, лишь бы не принимать ежедневно лекарства для профилактики сердечно-сосудистых заболеваний, и насколько сильно постоянный прием медикаментов снижает качество жизни пациентов. Задавались вопросы о том, какой частью жизни они гипотетически готовы пожертвовать, чтобы избежать необходимости ежедневно принимать таблетки, сколько денег они готовы за это заплатить, а также какой риск смерти считают приемлемым в этой ситуации.
Выявлено несколько тревожных моментов:
– каждый третий участник был готов пожертвовать частью своей жизни, чтобы только не принимать лекарства каждый день, 8 % респондентов готовы отдать целых два года жизни, 21 % — согласны жить на неделю-год меньше, зато 70 % не хотят жить меньше и готовы регулярно пить таблетки; – почти 13 % были готовы к минимальному риску смерти, лишь бы не принимать лекарства ежедневно, 9 % отвечавших готовы к 10%-ному риску смерти, зато 62 % участников опроса в принципе не согласны рисковать здоровьем и предпочтут регулярный прием препаратов;
– 21 % опрошенных готовы заплатить 1000 долларов, чтобы избавиться от необходимости постоянно пить таблетки, 43 % не согласны платить ни гроша, остальные предпочли торговаться.
Кокрановский обзор и другие опросы
20 ноября 2014 года в издании Cochrane Library вышел обзор, авторами которого обобщены данные 182 исследований приема лекарственных средств. Результаты неутешительные: почти половина участников опросов не соблюдают рекомендации врачей. Это в равной степени касается и больных простудой, и ВИЧ-инфицированных. Кто-то бросает пить таблетки раньше срока, кто-то забывает, как часто и в какое время суток это надо делать, не желая при этом заглянуть в инструкцию для уточнения. Так, до 30 % больных в Австрии не идут в аптеку, получив рецепт на лекарство.
Что касается России, то у нас лишь 48 % людей, страдающих повышенным артериальным давлением, принимают антигипертензивные препараты, а эффективно лечатся и того меньше — 19 %. По данным других российских исследований, примерно в 50 % случаев необъяснимых неудач в нормальном лечении пациент просто не принимал лекарства или делал это неправильно. Еще четверть неуспеха относят на долю невыполнения других рекомендаций (диета, режим сна, гигиены, стрессы и т.д.). 12 % — генетически и экологически обусловленные причины (например, невозможность сменить место жительства при астме). Причины 8 % неудач в лечении связаны с медслужбой (здесь и врачебные ошибки, и ошибки медсестер, отсутствие санитарок, несвоевременные приезды скорой, качество питания в стационарах, отсутствие там горячей воды и т.д.). 5 % отводится на другие, более редкие причины.
Понимаете? Половина случаев «плохого» лечения лежит в основном на совести самих пациентов!
Почему пациенты боятся лекарств?
Чаще всего все причины кроются в менталитете больного.
- «Одно лечат, другое калечат». Это мнение подтверждает и прочитанная аннотация к лекарству (где русским по белому указаны побочные эффекты и риски), и расхождения в назначениях, полученных у разных врачей. К тому же, если осмотр врача и выписанный им рецепт уже сами по себе успокоили в достаточной мере тревогу пациента, то для него необходимость строгого соблюдения назначений теряет свою актуальность.
- «Организм привыкнет, и лекарство перестанет помогать». Для врачей — забавная отговорка. Но действительно, иногда несмотря на аккуратный прием препаратов, организм выкидывает неожиданные фортели: повышается давление, усиливается тремор, — в общем, состояние ухудшается. И психика больного человека бунтует: он себя так ограничивал, так дисциплинированно выполнял все назначения — а тут!
- «У меня своя голова на плечах». Чаще всего мнение о способностях контролировать свой организм у больного крайне преувеличено. Парадоксальным образом обычно это сочетается с уважением к врачу, нежеланием «огорчить» или «обидеть» старающегося помочь доктора. Но хочется и какой-то свободы действий! В этом случае, к сожалению, включаются механизмы защиты сознания, и пациент старается обмануть врача.
Например, сотрудники Университета Клемсона в Южной Каролине подсчитали, что почти половина пациентов скрывают от своих врачей данные, необходимые для назначения правильного лечения. Так, участники исследования рассказывали врачам о состоянии здоровья, в то время как у медиков уже были сведения об их реальном самочувствии. Пациенты скрыли 40 % важной информации, в основном касающейся их личной жизни.
Нашлись причины вполне объяснимые: стыдно признаться, что был избит, дело касалось супружеской измены, была необходимость получить водительские права и т.д. Но обнаружились и совершенно невероятные, с точки зрения врачей, вещи:
– пациент стонет от боли и утверждает, что у него совсем-совсем ничего не болит;
– пациентка обижается на сам факт расспроса и начинает врать в отместку;
– пациент опрашивает соседа в очереди и сообщает врачу его симптомы, умалчивая о своих.
Там же приводится интересное обоснование обнаруженной иррациональности. Самооценка человека зависит от того, насколько он соответствует своему идеальному Я. «Я успешен, я красив, я независим, я самый лучший, у меня всё хорошо». ( «How are you? Fine!».) На приеме у врача этот шаблон самым позорным образом ломается. Пациент вынужден выглядеть хуже в собственных глазах, он может начать испытывать стыд и неловкость, а вдобавок обязан вслушаться в ощущения своего тела ради точного изложения симптомов. Как минимум половине пациентов это активно не нравится. И они уверены, что всю подноготную врачу не выложат ни за что и никогда.
Итог? Неутешительный: принимающий препараты больной ТОЧНО знает, что лечение «неправильное», так как доктор основывался на заведомо ложных исходных данных, — и перестает принимать назначенные препараты.
При каких заболеваниях принимать препараты приходится постоянно?
Список заболеваний, когда человек пожизненно «сидит на таблетках», крайне широк. В первую очередь это хронические болезни, угрожающие жизни пациента. Среди них сердечно-сосудистые (атеросклероз, артериальная гипертензия и т.п.), эндокринные (гормондефицитные состояния, сахарный диабет и т.п.), онкологические и психические заболевания.
Чем отличаются российские пациенты от своих зарубежных собратьев по несчастью?
Ничем. Как доказали ученые, половина случаев невыполнения назначений врача кроется в глубинных «вывертах» психики пациента и никакого отношения к стоимости лечения, доступности лекарств или качеству жизни отношения не имеет. Отмечается только, что россияне излишне увлекаются «народной» медициной, пытаясь лечить все заболевания тем, что находится «под рукой». И чаще всего в зоне доступности оказываются спиртосодержащие жидкости, а это — особенности национальной кухни, скажем так.
Как повысить лояльность пациента к назначенному лечению?
Сейчас в руках у врача имеется один-единственный козырь, и он называется «угроза жизни» — практически все врачи применяют метод запугивания как самый эффективный. Но профессор Корнеллского университета Брайан Уонсинк проанализировал рекомендации официальных служб населению и пришел к следующим выводам:
- Если благодаря выполнению предписания человек обязательно получит пользу, нужно формулировать совет позитивно («вы проживёте на 7 лет дольше, если будете принимать лекарство регулярно»).
- Если не совсем ясно, насколько высоки риски, советовать тоже лучше в положительном ключе — тогда рекомендацию проще будет понять («те, кто не принимает гипотензивные препараты, больше подвержены риску инсульта»).
- Большинство людей не интересуется деталями. Негативные советы могут быть эффективны только для тех, кто хочет знать всё в подробностях («если хотите жить парализованным — не принимайте лекарство»).
В заключение
Как говорил знаменитый немецкий врач-психиатр Эрнст Кречмер: «Дóктора приглашают не для того, чтобы он просто пожал плечами…». Вышеприведенные исследования — серьезный сигнал для работников социальных служб и врачей. Чтобы действительно улучшить жизнь людей, стоит подбадривать их и говорить им о положительных сторонах регулярного приема медикаментов, а не запугивать. Рекламщики это уже поняли. Поймут ли это коллеги и окружение больного хроническим заболеванием?
Источник
Путь лекарства
16 октября 2018
Путь лекарства
Создание нового лекарства требует большого количества ресурсов и времени. Невозможно предугадать успешность результата: подходящее, казалось бы, вещество, может дать сбой на любом этапе.
Автор
Редакторы
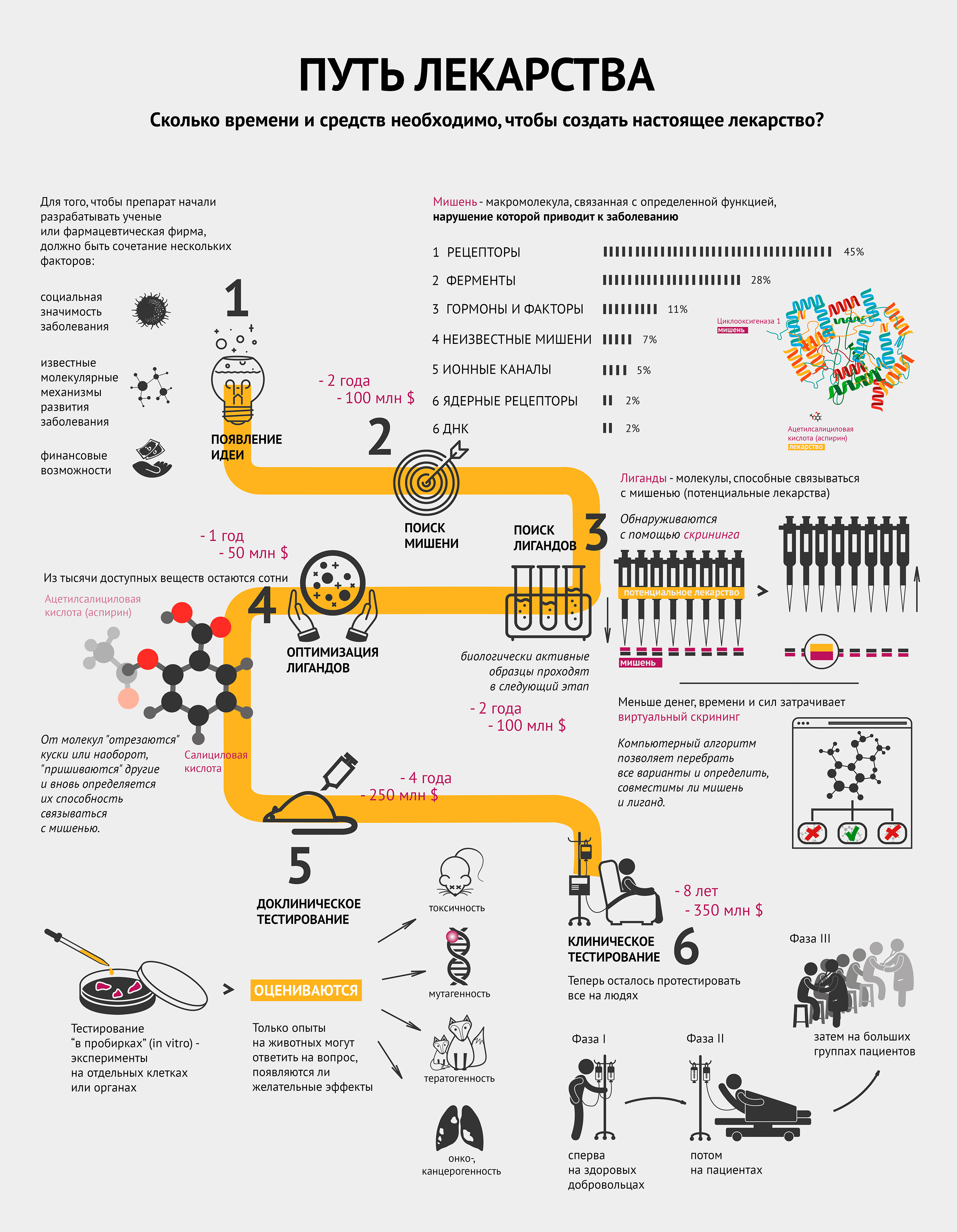
Инфографика на конкурс «био/мол/текст»: Казалось бы, для читателей «Биомолекулы» нет ничего понятнее, чем процесс создания лекарства. Однако почти никто не делал из этого инфографику — для смертных попроще. Вкратце — отсюда вы узнаете, сколько времени занимает процесс создания лекарства и насколько это недешево. И может быть, догадаетесь, что, если по телевизору сказали, что ученые обнаружили вещество, способное победить рак какую-нибудь заразу, то еще ох как рано бежать в аптеку в надежде купить новое лекарство.
Конкурс «био/мол/текст»-2018

Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий выступил медико-генетический центр Genotek.
Да здравствует идея!
Для того чтобы препарат начали разрабатывать ученые или фармацевтическая фирма, должно быть сочетание нескольких факторов [1]:
- социальная значимость заболевания;
- известные молекулярные механизмы развития заболевания;
- финансовые средства и возможности по созданию конкретного лекарства.
Другими словами, должна появиться идея.
Операция «Мишень»
Совместными усилиями группа ученых выбирает мишень и способ воздействия на нее для лечения или предотвращения заболевания.
Мишень — это биологическая макромолекула, связанная с определенной функцией, нарушение которой приводит к заболеванию [2]. Чаще всего мишенями являются белки — рецепторы и ферменты. Инфографика демонстрирует, какие макромолекулы чаще всего становятся мишенями [2]. Забегая вперед, стоит отметить, что затем к мишени подбирают вещество — лекарство. Самый распространенный пример — циклооксигеназа 1 (мишень) и ацетилсалициловая кислота (аспирин) (лекарство) — тоже проиллюстрирован (см. также видео).
Видео. Лекция Валентина Табакмахера «Драг-дизайн. Современный подход к созданию лекарств».
На поиски лигандов
После того, как ученые нашли мишень, им нужно понять, чем в нее целиться. Лиганд (потенциальное лекарство) — это химическое соединение (как правило, низкомолекулярное), специфически взаимодействующее со своей мишенью и тем самым влияющее на процессы внутри клетки [2].
Исследование всех возможных веществ, конечно, нереально: существует не менее 10 40 лигандов. Поэтому на структуру потенциальных лигандов накладывают ряд ограничений, которые существенно сужают поиск. В качестве отправной точки обычно используют библиотеки соединений, которые создаются специализированными компаниями по условиям, заданным разработчиком, или уже имеются в арсенале фармацевтической фирмы. Такие библиотеки могут содержать миллионы веществ [3].
Воздействуют ли выбранные лиганды на мишень, помогает определить скрининг. Он бывает лабораторным (in vitro) или компьютерным (in silico). В случае с лабораторным скринингом на особые предметные стекла — плашки, содержащие в тысячах микролитровых лунок тестовую систему, например молекулы белка-мишени или целые клетки (при необходимости — генетически модифицированные), — робот раскапывает из пипеток исследуемые вещества, следуя заданной программе. Потом происходит считывание данных, говорящее о том, в какой лунке обнаружена биологическая активность. Детектор может определять ее по радиоактивному сигналу, флюоресценции, поляризации света и многим другим параметрам [3].
Сокращай, оптимизируй!
Из тысяч доступных веществ с более-менее определенными свойствами необходимо выбрать сотни молекул, способных после дальнейшей модификации и испытаний на бактериях или культурах клеток дать десятки так называемых кандидатных соединений, предназначенных для доклинических исследований, включая тестирование на животных.
Оптимизация может заключаться в «отсечении» части известного лиганда, или наоборот, добавлении к нему новых элементов и новой проверке на взаимодействие с мишенью. Возвращаясь к аспирину: он получился из салициловой кислоты путем добавления ацетильной группы.
Тестировали, тестировали, да вытестировали
Отобранные соединения сначала тестируются в биохимико-фармакологических исследованиях или экспериментах на клеточных культурах, изолированных клетках и изолированных органах. Так как эти модели не способны полностью воспроизвести весь комплекс биологических процессов в настоящем организме, любое потенциальное лекарство тестируется на животных. Только опыты на животных могут ответить на вопрос, появляются ли желательные эффекты в нетоксичных или малотоксичных дозах.
Исследование токсичности призвано оценить:
- токсичность при кратковременном и длительном применении;
- возможность генетических повреждений (генотоксичность, мутагенность);
- возможность развития опухолей (онко- и канцерогенность);
- возможность рождения больного плода (тератогенность).
На животных исследуемые соединения испытываются также на поглощение, распределение, метаболизм и выделение (фармакокинетика) [4].
После этого этапа отсева на стадию клинических испытаний на людях остается в лучшем случае 1−3 препарата (напомню, что изначально было примерно 1000 потенциальных лекарств!).
Выходи на рынок!
Клиническое тестирование включает в себя несколько фаз, которые иллюстрирует инфографика [5].
Сначала проводится исследование новых препаратов на здоровых лицах с целью определить, наблюдаются ли у человека эффекты, обнаруженные в тестах на животных, и выявить взаимоотношения между дозой и эффектом.
Потом потенциальный новый препарат апробируется на избранных пациентах для определения терапевтической эффективности при заболевании, для которого он предназначен. Положительное действие должно быть явным, а нежелательные эффекты приемлемо малы.
Далее к исследованию привлекаются большие группы пациентов, с помощью которых исследуемое лекарство сравнивается со стандартным лечением по исходам терапии [4].
В процессе клинических испытаний многие новые лекарства признаются негодными к применению.
Решение одобрить новый препарат принимает национальный регулирующий орган (в России — Фармкомитет МЗ РФ). Заявители (фармацевтические компании) представляют в регулирующий орган полный комплект документации преклинических и клинических испытаний, в которых полученные данные об эффективности и безопасности удовлетворяют установленным требованиям и предполагаемую форму выпуска продукта (таблетки, капсулы и т.д.)
После получения одобрения новое лекарство может продаваться под торговой маркой и, таким образом, становится доступным для назначения врачами и распространения в аптеках. Параллельно идет разработка технологического процесса производства лекарственного средства, требований к качеству, методов анализа.
По мере распространения препарата за ним продолжается наблюдение. Окончательное суждение о соотношении «польза—риск» нового лекарства может быть сделано только на основании долговременного опыта его применения. Таким образом, определяется терапевтическая ценность нового лекарственного препарата.
В разных случаях процесс разработки нового лекарства от идеи до реализации занимает примерно от 5 до 18 лет. Суммарная стоимость разработки, с учетом препаратов, не достигших рынка, часто превышает 1 млрд долларов (до 2,5 млрд в среднем) [6].
Источник